
Back عطرية Arabic Aromatiklik termini Azerbaijani অ্যারোম্যাটিসিটি Bengali/Bangla Aromatičnost BS Aromaticitat Catalan Aromaticita Czech Ароматлăх CV Aromatizität German Αρωματικότητα Greek Aromaticity English
In die chemie is aromatisiteit 'n eienskap van sikliese (ringvormige), plat strukture met pi-bindings in resonansie (diegene wat gedelokaliseerde elektrone bevat) wat verhoogde stabiliteit verleen in vergelyking met ander geometriese of verbindingsrangskikkings met dieselfde stel atome. Aromatiese ringe is baie stabiel en breek nie maklik uitmekaar nie. Organiese verbindings wat nie aromaties is nie, word as alifatiese verbindings geklassifiseer. Sulke verbindings kan ringstrukture insluit, maar slegs aromatiese ringe het beter stabiliteit.
Aangesien die mees algemene aromatiese verbindings afgeleides van benseen is ('n aromatiese koolwaterstof wat algemeen voorkom in petroleum en die distillate daarvan), word die woord "aromaties" soms informeel gebruik na benseenderivate, en dit is dus was so die eerste keer gedefinieer. Nietemin bestaan daar baie nie-benseen aromatiese verbindings. In lewende organismes, byvoorbeeld, is die mees algemene aromatiese ringe die dubbelringbasisse in RNS en DNS. 'n Aromatiese funksionele groep of ander substituent word 'n arielgroep genoem.

Die vroegste gebruik van die term aromaties was in 'n artikel deur die Duitse chemikus August Wilhelm von Hofmann in 1855.[1] Hofmann het die term gebruik vir 'n klas benseenverbindings, waarvan baie reuke (aromas) het, in teenstelling met suiwer versadigde koolwaterstowwe. Aromatisiteit as 'n chemiese eienskap hou geen algemene verband met die reukeienskappe van sulke verbindings nie, hoewel chemici soos Hofmann in 1855, voordat die struktuur van benseen of organiese verbindings verstaan is, begin verstaan het dat geurige molekules van plante, soos terpeen, chemiese eienskappe het wat ons vandag herken en is soortgelyk aan onversadigde petroleumkoolwaterstowwe soos benseen.
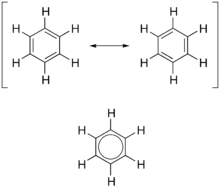
In terme van die elektroniese aard van die molekule, beskryf aromatisiteit 'n gekonjugeerde stelsel wat dikwels gemaak word van afwisselende enkel- en dubbelbindings in 'n ring. Hierdie konfigurasie laat toe dat die elektrone in die molekule se pi-stelsel om die ring gedelokaliseer word, wat die molekule se stabiliteit verhoog. Die molekuul kan nie deur een struktuur voorgestel word nie, maar eerder 'n resonansiebaster van verskillende strukture, soos met die twee resonansiestrukture van benseen. Hierdie molekules kan nie in een van hierdie voorstellings gevind word nie, met die langer enkelbande op een plek en die korter dubbele binding op 'n ander plek. Die molekuul vertoon eerder bindingslengtes tussen die van enkel- en dubbelbindings.
Hierdie model van aromatiese ringe, naamlik die idee dat benseen gevorm is uit 'n ses-ledige koolstofring met afwisselende enkel- en dubbelbindings (sikloheksatrien), is ontwikkel deur die Duitse organiese chemikus August Kekulé. Die model vir benseen bestaan uit twee resonansievorme, wat ooreenstem met die dubbel- en enkelbinding wat bo-op mekaar is om ses een-en-'n-half-bindings te produseer. Benseen is 'n meer stabiele molekuul as wat verwag sou word sonder om die ladingdelokalisering in ag te neem.
- ↑ Verwysingfout: Invalid
<ref>tag; no text was provided for refs namedHofmann1855
© MMXXIII Rich X Search. We shall prevail. All rights reserved. Rich X Search